1. CONCEPTO DE QUIMICA
La química es la ciencia que estudia la materia, su estructura, sus propiedades y sus transformaciones, así como las leyes que rigen éstas. La química es una ciencia natural que se basa en hechos experimentales (ciencia fáctica).
Es muy frecuente que a la química se le considere como una ciencia central, ya que para otras disciplinas (física, agronomía, biología, medicina, etc.), es esencial tener un conocimiento básico de esta ciencia. Efectivamente la química es una ciencia fundamental ya que sin ella la vida tendría un sentido efímero o sencillo.
En comparación con otros temas, es común creer que la química es más difícil. Hay algo de justificación para esta creencia: por un lado, la química tiene un vocabulario muy especializado. En todas las conversaciones se escuchan términos que tienen relación con la química, aunque no se utilicen en el sentido científico correcto (electrónica, reacción en cadena, explosión, fermentar, etc.)
1.1 DIVISIÓN DE LA QUÍMICA
Esta ciencia, al tener un campo de estudio tan amplio, para su mejor estudio se divide como se muestra a continuación:
Mientras que la química inorgánica estudia las sustancias minerales (inanimadas); la química orgánica se encarga de los compuestos del carbono.
La química analítica utiliza técnicas adecuadas para determinar las sustancias que forman una muestra material (química cualitativa) y para determinar también las cantidades de dichas sustancias (química cuantitativa).
2. CONCEPTO DE MATERIA
Una idea bastante difundida y acepada de materia es: “Todo aquello que tiene masa y que ocupa un lugar en el espacio”.
Otro concepto más es “Todo lo que ocupa espacio, tiene una propiedad llamada masa y posee inercia”. Cada ser humano es un objeto material. Todos ocupamos espacio y describimos nuestra mas por medio de una propiedad relacionada con ella, nuestro peso.
Otro de los conceptos de tipo filosófico es “Materia es todo aquello que se encuentra en movimiento, y no puede moverse de otro modo que en el espacio y en el tiempo”. La materia puede existir de dos modos: Concentrada o localizada y llamada sustancia; ó Dispersa o llamada Campo.
La sustancia es entonces materia concentrada y el campo es materia dispersa.
2.1 PROPIEDADES DE LA MATERIA
2.1.1 Propiedades Generales: Son aquellas que se encuentran presentes en todos los cuerpos sin excepción: masa, volumen, impenetrabilidad, porosidad, etc.
2.1.2 Propiedades Particulares: Son aquellas que se encuentran presentes solo en algunos cuerpos: dureza, maleabilidad, viscosidad, tenacidad, etc.
Las propiedades particulares pueden ser de tipo físicas o químicas
a) Propiedades Físicas: No cambian la estructura interna, es decir no crean nuevas sustancias. A su vez se dividen en Intensivas y Extensivas
*Intensivas:Estas propiedades no dependen de la cantidad de masa o materia (el color, sabor, densidad, temperatura, etc.)
6.2 FENÓMENO QUÍMICO: Son aquellas transformaciones que cambian la naturaleza de la materia de foma permanente, es decir cambian su estructura intima transformándose en nuevas sustancias y no son reversibles.
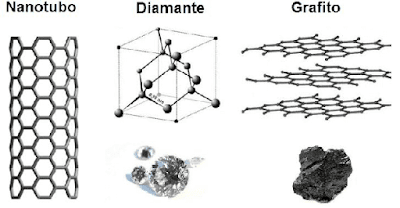
6.3 FENÓMENO ALOTRÓPICO: Son aquellas transformaciones de una misma sustancia en la misma fase, pero con propiedades diferentes tanto de estructura como de forma.
B) Cuántas mezclas se tienen en la siguiente relación:
C) Qué proposiciones son correctas
D) Cuántos de las siguientes sustancias no presentan alotropía
E) Indicar cuales son fenómenos físicos
*Extensivas:
Estas propiedades dependen de la cantidad de masa o materia (presión, energía, inercia, etc.)
b) Propiedades Químicas: Cambian la estructura interna, es decir crean nuevas sustancias (inflamabilidad, corrosión, ph, etc.)3. CLASIFICACIÓN DE LA MATERIA
4. ESTADOS DE AGREGACIÓN DE LA MATERIA
La materia se presenta en tres fases llamados estados de agregación molecular. Éstos estados dependen de las fuerzas intermoleculares existentes los cuales son la fuerza de cohesión y la fuerza de repulsión.
De la relación que guarden entre si éstas fuerzas, dependerá el estado de la materia: ESTADO SOLIDO, ESTADO LIQUIDO Y ESTADO GASEOSO
|
FASE |
FORMA |
VOLUMEN |
FUERZAS INTERMOLECULARES |
|
SÓLIDO |
INVARIABLE |
INVARIABLE |
Fc >>Fr |
|
LÍQUIDO |
VARIABLE |
INVARIABLE |
Fc<>Fr |
|
GASEOSO |
VARIABLE |
VARIABLE |
Fc<<Fr |
Un estado especial de la materia es el plasmático y se presenta en lugares donde las temperaturas son elevadas. El plasma es una mezcla de iones positivos y electrones libres.
Los cuerpos pueden sufrir cambios de estado o fases al variar su presión o temperatura, manteniéndose incluso en una misma fase.
La materia a medida de la reducción de su tamaño se puede dividir sistemáticamente mediante métodos mecánicos, físicos, químicos, nucleares, etc., y se puede tener las siguientes divisiones:
Fenómeno es todo aquello que sufre la materia y que son captados por nuestros sentidos.
6.1 FENÓMENO FÍSICO: Son aquellas transformaciones en un cuerpo que no cambian la naturaleza de la materia de la cual esta constituida, es decir no cambian su estructura íntima y son fácilmente reversibles.
6.2 FENÓMENO QUÍMICO: Son aquellas transformaciones que cambian la naturaleza de la materia de foma permanente, es decir cambian su estructura intima transformándose en nuevas sustancias y no son reversibles.
6.3 FENÓMENO ALOTRÓPICO: Son aquellas transformaciones de una misma sustancia en la misma fase, pero con propiedades diferentes tanto de estructura como de forma.
RETANDO TU APRENDIZAJE
A) Del siguiente listado de propiedades, cuantas son extensivas y cuantas son intensivas:
1. Inercia
2. Color
3. Densidad
4. Área
5. Calor latente de fusión
2. Color
3. Densidad
4. Área
5. Calor latente de fusión
B) Cuántas mezclas se tienen en la siguiente relación:
1. Aire
2. Bronce
3. Latón
4. Alcohol 70°
5. Mercurio
2. Bronce
3. Latón
4. Alcohol 70°
5. Mercurio
C) Qué proposiciones son correctas
1. El oro es mas dúctil que el hierro
2. La dureza es una propiedad particular de la materia
3. La ebullición se da a cualquier temperatura
4. La evaporación es un fenómeno de superficie
2. La dureza es una propiedad particular de la materia
3. La ebullición se da a cualquier temperatura
4. La evaporación es un fenómeno de superficie
D) Cuántos de las siguientes sustancias no presentan alotropía
1. Carbono.
2. Fósforo.
3. Azufre.
4. Oxígeno.
5. Potasio.
6. Sodio.
2. Fósforo.
3. Azufre.
4. Oxígeno.
5. Potasio.
6. Sodio.
E) Indicar cuales son fenómenos físicos
1. Solución de azúcar en agua
2. Fermentación del vino
3. Explosión de la nitroglicerina
4. Destilación del petróleo
5. Oxidación de barra metálica
2. Fermentación del vino
3. Explosión de la nitroglicerina
4. Destilación del petróleo
5. Oxidación de barra metálica















No hay comentarios:
Publicar un comentario
Envíanos tu opinión